Составим уравнения реакций. 6NaOH+2Al=Na3AlO3+2H2 .Данная реакция идет за счет амфотерных свойств алюминия.Вторая реакция будет идти без выделения газа. По формуле количества вещества объём делим на молярный объём 2.8:22.4 и получаем 0.125 моль. Дальше по коэффициентам узнаем количество Алюминия ,а затем и массу в соединение .0,125 делим на 3(перед водородом) и умножаем на 2(перед алюминием) ,а полученное число(0.083 примерно) умножаем на 27(молярная масса алюминия) . Узнаем массу меди 26-2.25=23.75 . А массовую долю (омегу) узнаем путем выражения 23,75(масса меди) делим на 26(общая масса) и умножаем на 100(так как в процентах) .В конце мы получаем ответ около 91 процент
Решение. По закону действующих масс скорость гомогенной химической реакции пропорциональна произведению молярных концентраций реагирующих веществ, возведенных в степени их стехиометрических коэффициентов. Увеличивать концентрации реагирующих веществ можно за счет повышения давления в сосуде.
Обозначим начальные концентрации молекул A2 и В через а и b соответственно:
Скорость реакции равна:
ν1 = k·[А2] ·[В]2 = k·а ·b2.
При увеличении давления в 6 раз концентрация каждого из веществ также увеличивается в 6 раз. В этом случае:
ν2 = k·(6а)·(6b)2 = 216k· a· b2=216· ν1
ответ: скорость реакции возрастет в 216 раз.
Объяснение:
1. З нерозчинним у воді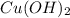 блакитного кольору утворює комплексну сполуку яскраво-блакитного кольору(прикладаю реакцію)
блакитного кольору утворює комплексну сполуку яскраво-блакитного кольору(прикладаю реакцію)
Висновок: для якісного визначення глюкози використовують важкі метали.
2. Етаналь можна визначити за до реакції "срібного дзеркала":
СН3-СНО + 2[Ag(NH3)2OH = CH3COOH + 2Ag(осад) + 4NH3 + H2O
на стінках пробірки утворюється тонкий шар срібла.
Висновок: для виявлення альдегідів можна узяти аміачний розчин аргентум(І) оксиду
Сахарозу можна виявити за реакцією:
С12H22O11 + Ca(OH)2 = C12H22O11*CaO + H2O
Cпостереження: утворення безбарвного розчину кальцій сахариту
Висновок: для виявлення сахарози необхідно узяти кальцій гідроксид
3. Для виявлення гідроксильної групи:
прикладаю фото
утворюється прозорий розчин купрум(ІІ) глюконату синього кольору
Для виявлення альдегідної групи:
CH2OH-(CHOH)4--CHO + Cu(OH)2 =(нагрівання) CH2OH-(CHOH)4-COOH + CuOH + H2O
За подальшого нагрівання утворюється осад цегляно-червоного кольору:
2CuOH = Cu2O(ocaд) + Н2О
блакитний купрум (ІІ) гідроксид розчиниться, а замість нього утвориться оранжевий осад купрум (І) гідроксиду, який за подальшого нагрівання набуде цегляно-червоного кольору.
Висновок: Щоб виявити глюкозу нам необхіден такий реактив як купрум (ІІ) гідроксид. Зазначимо те, що для виявлення альдегідної групи треба здійснити нагрівання