Нет.
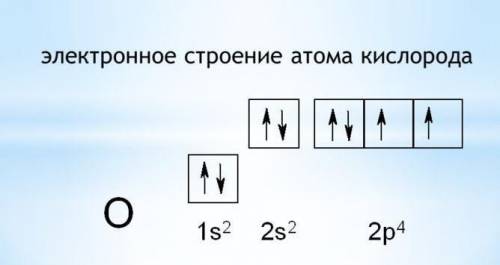
У Кислорода на внешнем уровне(2 уровень), в подуровне р-, два электрона без пары, за счёт них образуются стабильные две связи — валентность II всегда.
У Серы есть ещё и третий уровень, в котором есть s-, p- и d- подуровни. Поэтому у серы больше валентностей. В возбуждённом состоянии сера может проявлять валентность IV и VI кроме II.
Под n на рисунке подразумевается номер уровня.
16S 1s2 2s2 2p6 3s2 3p4 — валентность II, H2S;
16S* 1s2 2s2 2p6 3s2 3p3 3d1 — валентность IV, SO2;
16S** 1s2 2s2 2p6 3s1 3p3 3d2 — валентность VI, Na2SO4
На рисунке представлен внешний электронный уровень у серы в соединениях, указанных в качестве примеров.
У кислорода валентность II ВСЕГДА. Что в простом веществе O2, что в соединении H2O

Я не уверена, что ответ правильный. Но все, что мне пришло в голову, напишу.
Лед -твердое агрегатное состояние вещества. Молекулы вещества близки друг к другу и практически не двигаются.
Лед и вода -фаза перехода из твердого в жидкое состояние вещества. Молекулы начинают двигаться активнее, расстояние между ними увеличивается.
Вода -жидкое состояние вещества. Молекулы активно двигаются, между ними есть расстояние.
Лед и вода -фаза перехода из жидкого в твердое. Молекулы...как бы придвигаются ближе друг к другу.
И тд и тп. Я не знаю, то ли это.
Объяснение:
1)А; 2)В; 3)А; 4)В; 5)Б; 6)Б; 7)Г
Задача1:
Э2О3
О3 весят 16*3=48г/моль
пропорция: 48-30%
2Э-70%
2Э=112; Э=56 (см в табл Менд-это железо)
ответ: Fe2O3
Задача 2
2Са+О2t=2СаО(это в-во Х )
СаО+2НСl=CaCl2+ H2O (при н.У.)
СаCl2+K2CO3=2KCl+CaCO3(это в-во Y) реакция идет в растворе
СаСО3t=СаО+СО2