20.2 г
Объяснение:
Пишем обе реакции
2KNO₃ = 2KNO₂ + O₂ - реакция №1
2AgNO₃ = 2Ag + 2NO₂ + O₂ - реакция №2
Считаем массу кислорода в газовой смеси
m(O₂) = m(смеси) * w(O₂) = 9.4 * 0.5107 = 4.8 г (0.15 моль)
Пусть х моль - количество вещества кислорода в первой реакции, тогда 0.15 - х моль - количество вещества кислорода во второй реакции, а 2(0.15 - х) моль - количество вещества оксида азота. Поэтому
m(O₂) + m(NO₂) = M(O₂) * n(O₂) + M(NO₂) * n(NO₂) = 9.4 г
4.8 + 46 * 2 * (0.15 - x) = 9.4
x = 0.1 моль
Считаем массу нитрата калия
m(KNO₃) = n(KNO₃) * M(KNO₃) = 2n(O₂) * M(KNO₃) = 2 * 0.1 * 101 = 20.2 г
 моль
моль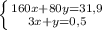
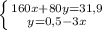

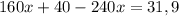

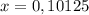 моль (это количество вещества Fe₂O₃)
моль (это количество вещества Fe₂O₃)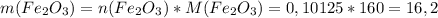 г
г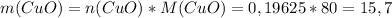 г
г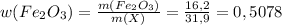 или 50,78% (где m(X) - это масса смеси)
или 50,78% (где m(X) - это масса смеси)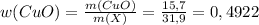 или 49,22%
или 49,22%
1.Na2CO3 + H2SO4 = Na2SO4 + CO2 + H2O
n(CO2) = n(Na2CO3) = 0,5 моль
V(CO2) = Vm*n = 22,4*0,5 = 11,2 л
3.
P->P2O5->H3PO4->Na3PO4->Ca3(PO4)2
1) 4P + 5O2 = 2P2O5
2) P2O5 + 3 H2O = H3PO4
3) H3PO4 + Na2SO4 = H2SO4 + Na3PO4
4) 2Na3PO4 + 3Ca(NO3)2=Ca3(PO4)2 (осадок) + 6NaNO3