Объяснение:
Формула летучего водородного соединения углерода имеет вид CH4. Это вещество органической природы, называется метан и является простейшим представителем класса предельных углеводородов.
СH4 + 2O2 = CO2↑ + 2H2O
a) n(CH4)=m(CH4):M(CH4)=500:16=31.25моль
M(CH4)=12+1*4=16г/моль
V(CO2)=n*Vm=31.25*22.4=700л
б)500см3 это 0,5л
n((CH4)=V(CH4):Vm=0.5:22.4=0.022моль
V(CO2)=n*Vm=0.022*22.4=0.5л
в) n(CH4)=m(CH4):M(CH4)=500:16000=0,03125моль
M(CH4)=12+1*4=16г/моль или 16 000мг/моль
V(CO2)=n*Vm=0,03125*22.4=0,7л
г)500м3 это 500 000л
n((CH4)=V(CH4):Vm=500000:22.4=22321,43моль
V(CO2)=n*Vm=22321,43*22.4=500000л
Молярный объем 1 моля газа при нормальных условиях всегда одинаков и равен 22,4л3 /моль
1Задача
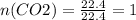 моль
моль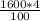 = 64 г
= 64 г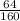 = 0.4 моль
= 0.4 моль
1) составляем уравнение реакции:
СnН2n-2 + 2НВr → СnН2nВr 2;
2) рассчитаем молярную массу углеводорода и продукта реакции:
М(СnН2n-2) = 14n – 2; М(СnН2nВr 2) = 14n + 160;
3) установим молекулярную формула углеводорода:
(14n + 160)/(14n – 2) = 4, n = 4;
Формула: С4Н6.
2) m(смеси) = m(CH4) + m(C2H2)
C2H2 + Br2 => C2H2Br2
CH4 + Br2 => нет реакции
2C2H2 +5O2 => 4CO2 + 2H2O
CH4 + 2O2 => CO2 + 2H2O
m (раст. вещ. Br2) =
n(Br2) =
n(C2H2) = 0.4 моль
m(С2Н2) = 0.4 * 26 = 10.4 г
0.4 *4 = 2 - 2x, где x = n1(C2H2)
n1(C2H2) = 0.2 моль
n(CH4) = 0.2 моль
m (CH4) = 0.2 * 16 = 3.2 г
m (смеси) = 3.2 + 10.4 = 13.6 г
ответ: m (смеси) = 13.6 г