Привіт! Зараз ми швидко усе запишемо:
A) Дано: водна емульсія аніліну, хлоридна кислота.
Запишемо рівняння реакції:
C₆H₅NH₂ + HCl → [C₆H₅NH₃]Cl
C₆H₅NH₂ + HCl → [C₆H₅NH₃]⁺Cl⁻
Це засвідчує про основні властивості, адже він реагує з кислотою, а з основами - ні.
Б) Дано: феніламоній хлорид, натрій гідроксид.
Запишемо рівняння реакції:
[C₆H₅NH₃]Cl + NaOH →C₆H₅NH₂ ↓+ NaCl + H₂O
[C₆H₅NH₃]⁺+Cl⁻ + Na⁺ + OH⁻ → C₆H₅NH₂ + Na⁺+Cl⁻ + H₂O
[C₆H₅NH₃]⁺ + OH⁻ → C₆H₅NH₂ + H₂O
Солі реагують з лугами з осаджуванням аніліну, бо металічний елемент забирає кислотний залишок, а гідроксильна група відбирає водень, що з'єднанний донорно-акцепторним зв'язком.
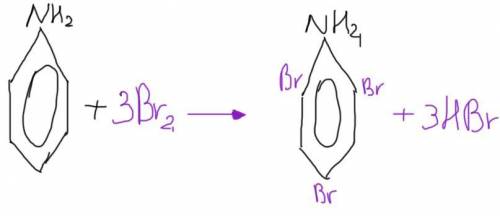
В) Дано: анілін, бромна вода.
*Дивимось на криво намальовану реакцію))
Якісною реакціює на анілін є CaOCl₂, бо розчин набуває фіолетового забарвлення.
Готово! Є питання? Запитуйте, з радістю відповім
*Поставте найкраще, будь ласка :)
Объяснение:
Качественными реакциями на ионы Fe3+ являются реакция тиоцианистыми соединениями и реакция с гексацианоферрат(II) калия (желтой кровяной солью):
Если к раствору соли железа(III) прибавить разбавленный раствор
тиоцианида калия KSCN или аммония NH4SCN, то образуется интенсивно-красное окрашивание:
Данную реакцию часто записывают упрощенно:
Fe3+ + 3KSCN = Fe(SCN)3 + 3K+
кроваво-красное
Другим реактивом на ион Fe3+ служит комплексное соединение
гексацианоферрат(II) калия «желтая кровяная соль»:
K4[Fe+2(CN)6] + Fe+3Cl3 = 3KCl + KFe+3[Fe+2(CN)6]
желтая кровяная соль берлинская лазурь
густой синий цвет
Реактивом на ионы Fe2+ Fe3+ может служить и раствор щелочи.
При действии щелочи на раствор солей железа(II) выпадает белый осадок гидроксида железа (II):
FeSO4 + 2KOH = Fe(OH)2↓ + K2SO4
Но такая реакция возможна только при полном отсутствии кислорода в растворе. В противном случае происходит постепенное окисление Fe(OH)2 до Fe(OH)3 и окраска осадка становится сначала грязно-зеленой, затем зеленовато-черной и лишь через некоторое время осадок приобретает ржавый цвет, характерный для Fe(OH)3:
4Fe(OH)2 + 2H2O + O2 ──> 4Fe(OH)3
Если же щелочь добавить в раствор, содержащий ионы Fe3+
то сразу выпадает красно-бурый осадок Fe(OH)3 :
FeCl3 + 3NaOH = Fe(OH)3↓ + 3NaCl
красно-бурый осадок
n=T/T1/2=16/8=2
2) Далее подставляем под формулу
m(нерас)=m(общ)/2 в степени n
m(нерас)=100%/4=25%
3) Теперь найдем суолько распалось 100%-25%=75%