К раствору хлорида кальция прильём раствор карбоната натрия (кальцинированной соды). О протекании реакции свидетельствует помутнение раствора — это выпал белый осадок карбоната кальция (мела):
Na2CO3 + CaCl2 = CaCO3↓ + 2NaCl.
Другой продукт реакции — хлорид натрия — хорошо растворим в воде и поэтому остаётся в растворе. При необходимости его можно получить выпариванием.
2. Соединим растворы сульфата натрия и нитрата калия. Можно ожидать, что будет протекать реакция в соответствии с уравнением:
Na2SO4 + 2KNO3 = 2NaNO3 + K2SO4.
Однако никаких изменений в растворе не происходит. В таком случае говорят, что реакция не протекает. Все четыре соли хорошо растворимы в воде.
3. Прильём к раствору кальцинированной соды соляную кислоту. Выделяется газ — это образовавшаяся в результате реакции обмена неустойчивая угольная кислота распадается на углекислый газ и воду:
4. К раствору щёлочи, подкрашенному несколькими каплями фенолфталеина, добавим азотную кислоту. Малиновая окраска раствора исчезает, что свидетельствует о протекании реакции:
KOH + HNO3 = KNO3 + H2O.
Как вы знаете, в результате взаимодействия оснований с кислотами образуются два продукта: соль и вода.
На основании приведённых реакций можно сформулировать необходимые условия для протекания реакций обмена в водных растворах. Реакция обмена протекает, если один из продуктов реакции — газ, осадок или вода.
х г 0,56 л
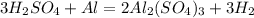
279 г 67,2 л
1. Найдем чистую массу кислоты,необходимую для образования 0,56 л водорода:
при взаимодействии 279 г кислоты выделяется 67,2 л водорода, а
при -- // -- // -- х г_____________________0,56 л, откуда
х=279*0,56/67,2=2,325 г
2. Учитывая,что полученная масса кислоты - это всего лишь 20% в растворе,тогда:
2,325 г кислоты - это 20%, а
у г раствора________100%, откуда у=2,325*100/20=11,625 или приблизительно 12 г
У водорода в водороде (бредово звучит ^_^) степень окисления равна 0 и в любом случае поменяется, так как больше нет веществ, у которых степень окисления равна 0.