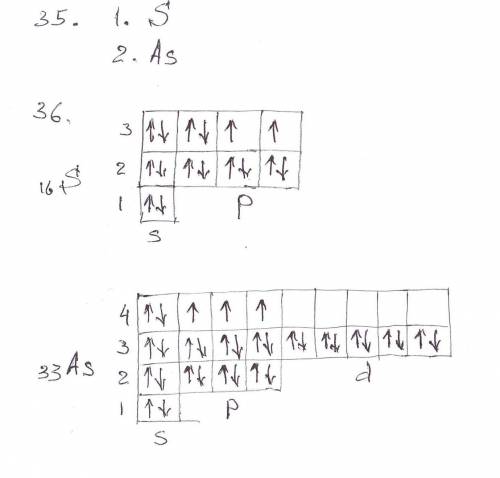
36. Дописать название подуровня и его номер. Записать химический знак элемента и перед ним поставить его порядковый номер. (См. в файл)
37. Номеру данного периода.
38. Номеру группы.
39. Количеством валентных электронов, т.е. электронов на внешнем слое.
40. Изменением строения их электронных оболочек. В каждом периоде происходит заполнение электронами внешнего энергетического уровня до восьми. Следовательно, электронные конфигурации наружных энергетических уровней периодически повторяются.
41. s-элементы - это элементы главной подгруппы I и II групп. По факту это элементы у которых заполняется s-уровень. В каждом периоде по 2 s-элемента.
42. р-элементы - это элементы III-VIII групп, главных подгрупп. Это элементы у которых заполняется р-уровень. Всего 6 р-элементов в каждом периоде (кроме первого, их там нет; и седьмого - хотя там тоже их 6 штук).
43. d-элементы - это элементы I-VIII групп, побочных подгрупп. Это элементы у которых заполняется d-уровень. В каждом большом периоде по 10 d-элементов.
Объяснение:
100,19g
Объяснение:
Признак реакции- осадок BaSO4
дано:m (K2SO4)= 75g
найти: m(BaSO4)-?
K2SO4+BaCl2=2KCl+BaSO4 (осадок)
n(K2SO4)= m(K2SO4)/M(K2SO4)= 75/174=0,43 моль
по реакции:
n(BaSO4)=n(K2SO4)=0,43 моль
тогда,
m(BaSO4)= n(BaSO4)*M(BaSO4)= 0,43* 233= 100,19 g