Запишем уравнения протекающих реакций:
(1)CaSO4 + 2HCl = CaCl2 + H2O + SO2
(2)CaCO3 + 2HCl = CaCl2 + H2O + CO2
Теперь анализируем. По условию, газ выделившийся в результате.....обесцвечивает раствор перманганата калия. Это будет окислительно - восстановительная реакция, нужно чтобы газ, вступающий в данную реакцию, был восстановителем - т.. находиться либо в низжей, либо в промежуточной степени окисления, рассмотрим образовавшиеся газы:
CO2 и SO2
Максимальная С.О. у углерода +4
Максимальная С.О. у серы +6
В CO2 С.О. углерода +4 - высшая, газ намс не подходит
В SO2 С.О. серы +4, а высшая +6, значит сера находится в промежуточной степени окисления, это то, что нам нужно. Пишем реакцию с перманганатом
(3)2KMnO4 + 5SO2 + 2H2O = K2SO4 + 2MnSO4 + 2H2SO4
По условию, дан кислый раствор перманганата, массой 158г, с массвой долей 10%, рассчитаем массу растворенного вещества в нем:
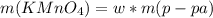 = 0,1*158г = 15,8г
= 0,1*158г = 15,8г
Рассчитаем количество вещества пермаганата:
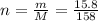 = 0,1моль
= 0,1моль
По уравнению реакции: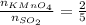 , значит n(SO2) = 5/2n(KMnO4) = 0,25моль
, значит n(SO2) = 5/2n(KMnO4) = 0,25моль
По уравнению реакции:
n(CaSO3) = n(SO2) = 0,25моль
Рассчитаем массу CaSO3
m = n*M = 0,25моль*120г/моль = 30г
m(CaCO3) = 30грамм
доли: w(CaSO3) = 50%, w(CaCO3) = 50%
1)Al2O3 + 6HCl → 2AlCl3 + 3H2O
(оксид алюминия + соляная кислота →хлорид алюминия + вода)
2) AlCl3 + 3NaOH →Al(OH)3 + 3NaCl
3Al + 3Cl + 3Na + 3OH → Al(OH)3 +3Na +3Cl
3Al + 3OH → Al(OH)3
(хлорид алюминия + гидрооксид натрия →гидрооксид алюминия + хлорид натрия)
Суммы коэффициентов в полном и сокращённом ионно- молекулярном уравнениях соответственно равны: а) 19 и 7
3) Al(OH)3 → Аl2О3+3Н2О
( гидрооксид алюминия →оксид алюминия + вода)
Степень окисления оксидов атомов элементов в оксиде алюминия: у алюминия ст.ок=+3 ; у кислорода ст.ок=-2(минус двум)
мол.масса=16(атомная масса кислорода)+64(а.м.меди)=80г/моль
Как-то так надеюсь,что верно)