а) 2-метилбутадиен-1,3
б) гексадиен-2,4
в) пентадиен-2,3
г) гексадиен-1,4
Объяснение:
Для начала необходимо найти самую длинную цепочку. Найдя её, начинаем отсчёт с того края, куда ближе двойные связи или разветвления (радикалы). В первом случае, от второго по счёту атома отходит радикал метил (CH₃), двойные связи отходят от первого и третьего по счёту атома. Атомов углерода в цепи, не захватывая радикал, всего 4, следовательно, мы рассматриваем бутадиен.
Если двойные связи находятся на равном расстоянии от обоих концов цепи, отсчёт можно начинать хоть с одного, хоть с другого конца.
Для того чтобы понять, какой перед нами алкадиен, необходимо посчитать количество атомов углерода в цепи и вспомнить гомологический ряд данных углеводородов. После названия вещества записывается нумерация тех атомов, от которых идёт двойная связь. Не забываем про порядок в рассматриваемой цепи.
Нашлось, по крайней мере два соединения, гидрида, в которых массовая доля водорода равна 12,5%:
гидрид лития LiH и гидрид кремния (силан) SiH₄.
Объяснение:
Массовая доля водорода в соединении с другим элементом составляет 12,5% или 0,125.
Тогда массовая доля неизвестного элемента в данном соединении равна 100% - 12,5% = 87,5% или 0,875.
Имеется некоторое соединение, гидрид элемента E состава EHₙ , где n - валентность неизвестного элемента E.
Массовая доля водорода и массовая доля элемента E в веществе:
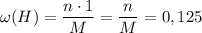 , где M - молярная масса вещества.
, где M - молярная масса вещества.
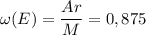
Найдем отношение массовых долей элементов:

Тогда относительная атомная масса элемента E равна Ar = 7n.
1) При n = 1 , Ar = 7, это литий, его валентность равна 1, гидрид имеет формулу LiH.
Сделаем проверку массовых долей лития и водорода:
M(LiH) = 7 + 1 = 8

Верно.
2) При n = 2, Ar = 14. Это азот, но азот в соединении с водородам проявляет валентность III. NH₃. Не подходит.
3) При n = 3, Ar = 21. Элемента с такой атомной массой нет. Не подходит.
4) При n = 4, Ar = 28. Это кремний, гидрид имеет формулу SiH₄ (силан)
Сделаем проверку массовых долей кремния и водорода:
M(SiH₄) = 28 + 4 = 32
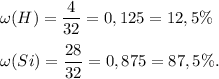
Верно.
Дано:
m(PhOH)p-p = 300г
w(PhOH) = 10% = 0,10
+m(NaOH) = 12г
Найти:
m(PhONa)
Решение:
m(PhOH) = 300*0,10 = 30г
PhOH + NaOH = PhONa + H₂O
Mr(NaOH) = 40 г/моль
Mr(PhOH) = 94 г/моль
Mr(PhONa) = 116 г/моль
Для реакции с 30г фенола необходимо натрия:
m(PhONa) =
ответ: m(PhONa) = 34,8г