Запишем уравнение реакции:
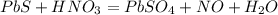
Расставим степени окисления и оставим только у тех элементов, что ее меняют:
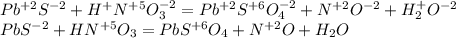
Запишем редокс:
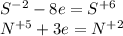
Расставим коэффициенты так, чтобы количество принятых e было равно кол-ву отданных:

Сера - восстановитель, окисление
Азот - окислитель, восстановление
Поставим соответствующие коэффициенты (3 и 8) перед молекулами в реакции:
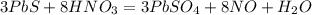
Уравняем по водороду, слева водорода 8, справа 2, значит перед водой коэффициент 4:
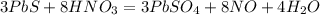
Уравнено!
Запишем уравнение реакции:
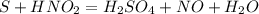
Расставим степени окисления и оставим только у тех элементов, что ее меняют:
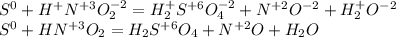
Запишем редокс:
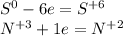
Расставим коэффициенты так, чтобы количество принятых e было равно кол-ву отданных:
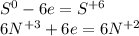
Сера - восстановитель, окисление
Азот - окислитель, восстановление
Поставим соответствующий коэффициент (6) перед молекулой в реакции:
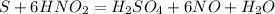
Уравняем по водороду, слева водорода 6, справа 2 в воде, 2 в кислоте, значит перед водой коэффициент 2:
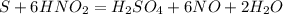
Уравнено!
S+O2=SO2;SO2+NaOH=Na2SO3+H2;Na2SO3+H2O=H2SO3+NaOH;H2SO3+O2=SO2+H2O