15.1
Al2(SO4)3 - сульфат аллюминия
Ba(NO3)2 - нитрат бария
NaAlO2 - метаалюминат натрия
K2CO3 - карбонат калия
FeCl3 - хлорид железа (III)
Na3AsO4 - арсенат натрия
AgI - йодид серебра
Na2SiO3 - силикат натрия
15.2
HNO2 - соотетствующим оксидом будет N2O3
Be(OH)2 - соотетствующим оксидом будет BeO
HIO3 - соотетствующим оксидом будет Cl2O5
H2CrO4 - соотетствующим оксидом будет CrO3
Cr(OH)3 - соотетствующим оксидом будет Cr2O5
15.3
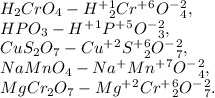
15.4
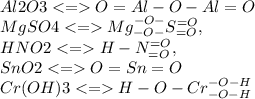
15.5
ZnSO4 → Zn(OH)2 → ZnCl2 → AlCl3 → Al(OH)3.
ZnSO4 +NaOH = Na2SO4 + Zn(OH)2;
Zn(OH)2 + 2HCl = ZnCl2 + 2H2O;
3ZnCl2 + 2Al = 2AlCl3 + 3Zn;
AlCl3 + 3NaOH = 3NaCl + Al(OH)3
ответ:5.6л
Объяснение:Відомо: ν(Na2СO3)=0,25 моль. Знайти: V(HNO3)-?
Розв'язування:
іб
Записуємо рівняння реакції.
0,25 моль х л
2HNO3 + Na2CO3 = 2NaNО3 + CO2↑+ H2O
1 моль 22,4 л
Над формулами речовин записуємо дані, що є за умовою задачі.
Мольні співвідношення речовин показують коефіцієнти рівняння. Прореагувало 1 моль натрій карбонату Na2СO3 з утворенням 1 моль вуглекислого газу СО2 (1 моль газу за н.у. займає об'єм 22,4 л).
Відповідні значення записуємо під формулами речовин у рівнянні реакції.
Складаємо пропорцію і розв'язуємо її.
0,25 моль / 1 моль = х л / 22,4 л, звідси
х л • 1 моль = 0,25 моль • 22,4 л
х=0,25 моль • 22,4 л / 1 моль
х=5,6 л.
Відповідь: V(СO2)=5,6 л.
іб
Записуємо рівняння реакції: 2HNO3+Na2CO3=2NaNО3+CO2↑+H2O
Мольні співвідношення речовин показують коефіцієнти рівняння. Прореагувало 1 моль натрій карбонату Na2СO3 з утворенням 1 моль вуглекислого газу СO2, кількості речовин однакові. Отже, якщо в реакцію вступає 0,25 моль натрій карбонату, то утворюється така ж кількість речовини вуглекислого газу, тому
v(СO2)=v(Na2CO3)=0,25 моль.
Знаходимо об'єм вуглекислого газу кількістю речовини 0,25 моль за формулою V=v•VM, де VM-постійна величина і за н.у. чисельно дорівнює 22,4 л/моль.
V(CO2)=v(CO2)•VM=0,25 моль•22,4 л/моль=5,6 л.
Відповідь: V(CO2)=5,6 л.
Mr(2Fe2O3)=2×(56×2+16×3)=160×2=320
40x
224320
x=40×320/224
x=57,1
4P+5O2=2P2O5
Mr(2P2O5)=2×(31×2+16×5)=2×142=284
40x
124284
x=40×284/124
x=91,6