77.8 г
Объяснение:
Формула железного купороса - FeSO₄·7H₂O. Его молярная масса состоит из молярных масс сульфата железа (152 г/моль) и семи молекул воды (18 * 7 = 126 г/моль) и составляет 152 + 126 = 278 г/моль. Так как расчет на 1 моль вещества, то можем сказать, что в 278 г купороса содержится 152 г сульфата железа. Тогда в 5 г купороса содержится (5 * 152) / 278 ≈ 2.734 г сульфата железа
Пусть взяли х г 5%-го раствора. Тогда масса сульфата железа в нем будет 0.05х г. Теперь это все подставим в формулу
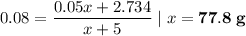
0.0167моль 0.0167моль
СН2(ОН)-СН2(ОН)-СН2(ОН)+ 3HNO3=CH2(O-NO2)-CH2(O-NO2)-CH2(O-NO2) +3H2O
1моль 1 моль
Определим кол-во вещества CH2(O-NO2)-CH2(O-NO2)-CH2(O-NO2)
n=m/M
n( CH2(O-NO2)-CH2(O-NO2)-CH2(O-NO2)) = 2.270/136=0.0167моль
M( CH2(O-NO2)-CH2(O-NO2)-CH2(O-NO2)) =136г/моль
Из уравнения реакции следует, что n(СН2(ОН)-СН2(ОН)-СН2(ОН))=n( CH2(O-NO2)-CH2(O-NO2)-CH2(O-NO2)) =0.0167моль
Найдем массу СН2(ОН)-СН2(ОН)-СН2(ОН)
m=n*M
m=0,0167*93=1.55г
m(СН2(ОН)-СН2(ОН)-СН2(ОН))=93 г/моль
ответ:1.55г