Кисень O2, вуглекислий газ СO2, озон O3 — важчі за повітря.
Щоб довести це, скористаємося наслідком із закону Авогадро. Порівняємо маси газів, що відповідають об’єму 22,4 л. Кількість речовини газів, що міститься у цьому об’ємі, дорівнює 1 моль, а маса дорівнюватиме молярній масі.
М(повітря) = 29 г/моль, М(O2) = 32 г/моль, М(СO2) = 44 г/моль, М(O3) = 48 г/моль.
Отже, маса 22,4 л кисню, взятого за нормальних умов, становитиме 32 г, а маса такого самого об’єму повітря — 29 г.
Відносна густина показує, у скільки разів один газ важчий за інший. Розрахуємо відносну густину кисню, вуглекислого газу, озону за повітрям.
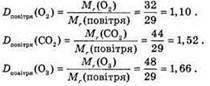
1. Найдем через плотность относительную молекулярную формулу вещества:
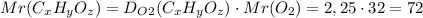
2. Теперь,вспомнив формулу по вычислению массовой доли элемента в веществе и выведя из нее n - количество атомов элемента,найдем количество атомов каждого:
а) n(C)=Mr(C_xH_yO_z)*w(C)/Ar(C)*100%=72*66,67/12*100=4
б) n(H)=Mr(C_xH_yO_z)*w(H)/Ar(H)*100%=72*11,11/1*100=8
в) n(O)=Mr(C_xH_yO_z)*w(O)/Ar(O)*100%=72*22,22/16*100=1
Выходит простейшая формула: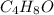
Если подставлять в общие формулы кислородсодержащих соединений,то получим: -это бутаналь
-это бутаналь
CuO+2HCl->CuCl2+H2O
CuCl2+2NaOH-> Cu(OH)2+2NaCl
Cu(OH)2->CuO+H2O (при t)
CuO+H2SO4->CuSO4+H2O