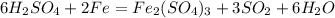
Ви вже знаєте, що серед сполук різних елементів окрему групу станов-
лять ті, що утворені Карбоном, — так звані органічні сполуки. З найважли-
вішими з них ви ознайомилися в поперед ніх класах, а докладно вивчити
органічні речовини в усій їхній багатоманітності зможете в окремому роз-
ділі органічної хімії. Цей підручник відкриє багато нового, досі невідомого
про природні й синтетичні сполуки, із яких виготовлено ваш одяг, які ви
вживаєте в їжу, які вас обігрівають і лікують, з яких, зрештою, побудовано
ваш організм.
Зміст кожної наступної теми і кожного наступного параграфа підручни-
ка ґрунтується на змісті попередніх. Намагайтеся зрозуміти логіку органіч-
ної хімії — і ви легко засвоїте навіть найскладніший матеріал. А знання
залежності властивостей органічних речовин від їхніх складу та будови да-
дуть вам змогу не лише пояснювати ці властивості, а й передбачати їх.
У вивченні хімії вам до структура підручника. Фактичний
матеріал про органічні сполуки викладається в рубриках: Склад і будова
молекул, Фізичні властивості, Хімічні властивості, Застосування,
Добування. Матеріал про хімічні властивості як найважливіший подано в
зручному вигляді: рівняння хімічних реакцій речовин згруповано в одному
місці, а пояснення цих реакцій наведено паралельно.
Кожна тема закінчується висновками, в яких узагальнено основ ний,
найважливіший матеріал. Наприкінці параграфів наведено завдання, за
до яких ви можете перевірити свої знання і розуміння вивченого.
Не лінуйтеся робити це систематично — і успіх у навчанні забезпечений. Не
нехтуйте також запитаннями, уміщеними в тексті параграфів.
Навички експериментування ви зможете розвинути, виконуючи різно-
манітні хімічні досліди. Прописи лабораторних робіт наведено в тексті па-
раграфів, а практичних робіт — наприкінці підручника.
Сподіваємося, що вивчення органічної хімії буде для вас цікавим і ко-
рисним.
Успіхів вам!
ответ:1)Из-за высокой химической активности кальций в свободном виде в природе не встречается.
На долю кальция приходится 3,38 % массы земной коры (5-е место по рас е среди металлов) после кислорода, кремния, алюминия и железа). Содержание элемента в морской воде — 400 мг/л[4].
2)Свободный металлический кальций получают электролизом расплава, состоящего из CaCl2 (75—80 %) и KCl или из CaCl2 и CaF2, а также алюминотермическим восстановлением CaO при 1170—1200 °C
4CaO+2Al=CaAl2O4+3Ca
3)Металл кальций существует в двух аллотропных модификациях. До 443 °C устойчив α-Ca с кубической гранецентрированной решеткой (параметр а = 0,558 нм), выше устойчив β-Ca с кубической объемно-центрированной решеткой типа α-Fe (параметр a = 0,448 нм). Стандартная энтальпия Delta H^0 перехода α → β составляет 0,93 кДж/моль.
При постепенном повышении давления начинает проявлять свойства полупроводника, но не становится полупроводником в полном смысле этого слова (металлом уже тоже не является). При дальнейшем повышении давления возвращается в металлическое состояние и начинает проявлять сверхпроводящие свойства (температура сверхпроводимости в шесть раз выше, чем у ртути, и намного превосходит по проводимости все остальные элементы). Уникальное поведение кальция похоже во многом на стронций (то есть параллели в периодической системе сохраняются)
4)1.Взаимодействие с кислородом и серой (при обычных условиях) .
2Са + O2 = 2СаO
Ca + S = CaS
2.Легко реагирует с галогенами.
Са + Cl2 = СаCl2
3.При нагревании реагирует с водородом, азотом, углеродом, кремнием и другими неметаллами.
Ca + H2 = CaH2
3Са+ N2 = Са3N2
Ca + 2C = CaC2
4.Расплавленный кальций может соединяться с другими металлами, образуя интерметаллиды (CaSn3, Ca2Sn).
5.Взаимодействие с водой.
Ca + 2H2O = Ca(OH)2 + H2↑
6.Взаимодействие с кислотами.
В реакциях с хлороводородной и разбавленной серной кислотой выделяется водород:
Са + 2HCl = СаCl2 + H2↑
Разбавленную азотную кислоту восстанавливают до аммиака или нитрата аммония:
4Ca + 10HNO3(разб. ) = 4Ca(NO3)2 + NH4NO3 + 3H2O
Восстанавливает концентрированную серную кислоту до H2S, а концентрированную азотную – до N2O.
7.Взаимодействие с оксидами и солями металлов:
V2O5 + 5Ca = 2V + 5CaO
Объяснение:
6H2SO4 + 2Fe = Fe2(SO4)3 + 3SO2 + 6H2O
Fe(0)-3e = Fe(+3) 2 в-ль, ок-ие
S(+6)+2e = S(+4) 3 ок-ль, в-ие