Таблица 11-1. <a href="/info/424373">Влияние хлорида</a> натрия на <a href="/info/149218">растворимость хлората</a> натрия Предварительное донасыщение щелоков поваренной солью перед подачей их в кристаллизатор необходимо для снижения растворимости хлората натрия и, следовательно, для более полного его выделения в процессе кристаллизации. [c.394]
Из данных видно, что растворимость увеличивается с повышением температуры. На растворимость ЫаСЮз в воде оказывает влияние присутствие хлорида натрия, при этом с увеличением концентрации хлорида натрия растворимость хлората натрия снижается. [c.146]
Хлорат калия растворяется в воде — при О °С — 3 вес. ч., а при 100 °С — 56,5 вес. ч. в 100 вес. ч. Растворимость хлората натрия в воде лучше при О °С — 80 вес. ч., а при 100 °С — 230 вес. ч. в 100 вес. ч. Хлораты (в особенности натрия) используют при окислении анилина в анилиновый черный и в производстве взрывчатых веществ и ядохимикатов. [c.138]
Растворимость хлората натрия в воде при различных температурах приведена ниже [c.146]
Аналогично растворимости хлората натрия растворимость КСЮз уменьшается в присутствии хлорида калия и сильно увеличивается с повышением температуры [c.146]
В табл. 7-3 приведена растворимость хлората натрия (в г/100 мл раствора) в растворах поваренной соли. [c.369]
Выделение кристаллического хлората. Получаемый после выпарки раствор подвергают кристаллизации в вакуум-кристаллизаторах, где охлаждение кристаллизуемого раствора происходит за счет испарения влаги. Кристаллы хлората натрия отделяют от раствора на центрифугах и в случае необходимости подвергают сушке, а маточные растворы возвращают в цикл для приготовле- ния исходного электролита. При работе по схеме без выпарки полученные растворы хлората натрия, содержащие 500 г/л Na lOg, подогревают до 40—50° С и насыщают хлоридом натрия для снижения растворимости хлората натрия. После насыщения раствора до 140—156 г/л Na l раствор подвергают кристаллизации в классифицирующем кристаллизаторе при охлаждении до —3—5° С. Охлаждение раствора осуществляется в противоточном холодильнике, охлаждаемом рассолом. Устройство классифицируемого кристаллизатора позволяет получать необходимый гранулометрический состав конечного продукта. [c.14
1. Спирти мають функціональну гідроксильну групу(-ОН), тільки одноатомні мають у своїй будові лише одну групу,а багатоатомні-дві або більше.
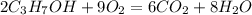
2.а) 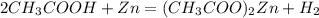 -ацетат цинка и водород(реакция замещения)
-ацетат цинка и водород(реакция замещения)
б) 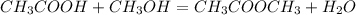 -метиловый эфир уксусной кислоты и вода(реакция обмена)
-метиловый эфир уксусной кислоты и вода(реакция обмена)
в) 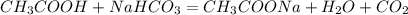 -ацетат натрия,вода и углекислый газ(реакция обмена)
-ацетат натрия,вода и углекислый газ(реакция обмена)
3. До складу твердих жирыв входять залишки насичених вищих карбонових кислот(стеаринової або пальмітинової),а до рідких-залишки ненасичених вищих карбонових кислот(олеїнової).Тверді жири - це тваринні жири(крім риб'ячого),а рідкі - рослинні(крім пальмового масла).Жири в живих організмах виконують енергетичну роль(при окисненні жирів вивільняється майже в два рази більше енергії,ніж при окисненні такої ж кількості вуглеводів або білків),будівельну(входять до складу біологічних мембран),захисну(жир підшкірної клітковини захищає від механічних ушкоджень внутрішні органи)
4. Сахароза - це типовий дисахарид,який складається із залишків глюкози і фруктози.Тверда кристалічна речовина,добре розчинна у воді,трохи солодша на смак від глюкози.Поширена у природі у цукровому буряці та цукровій тростині,з яких і видобувають цукор(сахарозу).В присутності концентрованної сульфатної кислоті гідролізує(тобто взаємодіє з водою),в результаті утворюються глюкоза і фруктоза:
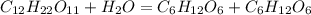
При повному окисненні утворюються вода і вуглекислій газ:
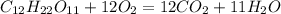
4P + 5O2 = 2 P2O5 соединение
ответ 1 и 4