ответ:
объяснение:
дано:
m (nh4cl) = 75 г;
найти:
m (nh3) - ?
решение:
1) составляем уравнение реакции согласно условию :
nh3 + hcl = nh4cl;
2) находим количество хлорида аммония, содержащееся в 75 граммах соли:
n (nh4cl) = m : m = 75 г : 53,5 г/моль = 1,4 моль;
3) составляем логическое равенство:
если 1 моль nh3 дает 1 моль nh4cl,
то x моль nh3 даст 1,4 моль nh4cl,
тогда х = 1,4 моль.
4) находим массу аммиака, затраченную на протекание реакции:
m (nh3) = n * m = 1,4 моль * 17 г/моль = 23,8 г;
ответ: m (nh3) = 23,8 г.

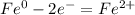
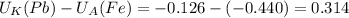 В (Вольт)
В (Вольт)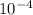 то ЭДС необходимо рассчитать с формулы Нернста:
то ЭДС необходимо рассчитать с формулы Нернста:![((U_{K})^o+ \frac{0,059}{n}lg[Me^{n+}]_k)-( (U_{A})^o)+ \frac{0,059}{n}lg[Me^{n+}]_a )](/tpl/images/0408/4708/bd0bf.png)
 В (Вольт)
В (Вольт)
Получение основных оксидов:
1. Окисление металлов при нагревании в атмосфере кислорода:
2Mg + О2 = 2МgО,
2Сu + О2 = 2СuО.
Этот метод практически неприменим для щелочных металлов, которые при окислении обычно дают пероксиды, поэтому оксиды Na2О, К2О крайне труднодоступны.
2. Обжиг сульфидов:
2CuS + ЗО2 = 2СuО + 2SО2,
4FeS2 + 11О2 = 2Fе2О3 + 8SО2.
Метод неприменим для сульфидов активных металлов, окисляющихся до сульфатов.
3. Разложение гидроксидов:
Cu(OH)2 = CuO + H2O
Этим методом нельзя получить оксиды щелочных металлов.
4. Разложение солей кислородсодержащих кислот:
BaCO3 = BaO + CO2
2Рb(NО3)2 = 2PbО + 4NO2+O2
4FеSО4 = 2Fe2O3 + 4SO4 + O2